塩基
酸と塩基 |
|---|
|
塩基(えんき、英: base)は化学において、酸と対になってはたらく物質のこと。一般に、プロトン (H+) を受け取る、または電子対を与える化学種[1]。歴史の中で、概念の拡大をともないながら定義が考え直されてきたことで、何種類かの塩基の定義が存在する。
塩基としてはたらく性質を塩基性(えんきせい)、またそのような水溶液を特にアルカリ性という。酸や塩基の定義は相対的な概念であるため、ある系で塩基である物質が、別の系では酸としてはたらくことも珍しくはない。例えば水は、塩化水素に対しては、プロトンを受け取るブレンステッド塩基として振る舞うが、アンモニアに対しては、プロトンを与えるブレンステッド酸として作用する。塩基性の強い塩基を強塩基(強アルカリ)、弱い塩基を弱塩基(弱アルカリ)と呼ぶ。また、核酸が持つ核酸塩基のことを、単に塩基と呼ぶことがある。
目次
1 アルカリ
2 塩基の定義
3 英語 Base の語源
4 出典
5 関連項目
アルカリ
アルカリ金属やアルカリ土類金属などの水酸化物、あるいはアンモニア、アミンなど水溶液のpHが7より大きく塩基性を示す物質を総称してアルカリ (英: alkali) と呼ぶ[2]。アラビアの科学者ジャービル・イブン=ハイヤーンが生み出した概念である(「アルカリ」は灰を意味するアラビア語に由来する)。また、アルカリ性の水溶液やアルカリ金属のことを、単にアルカリと呼ぶことがある。アルカリ性の化合物は基本的に苦味を呈す。
塩基の定義
以下に、それぞれの塩基の定義を概略のみ述べる。
- アレニウス塩基 (Arrhenius base)
アレニウスの定義による塩基。水に溶けたときに水酸化物イオン (OH−) を出す物質。下式において、水酸化ナトリウム (NaOH) はアレニウス塩基としてはたらいている。- NaOH⟶Na++OH−displaystyle ce NaOH -> Na^+ + OH^-
- ブレンステッド塩基 (Brønsted base)
ブレンステッド-ローリーの定義による塩基。プロトンを受け取る物質[3]。下式の反応で「B」、あるいは「B−」がブレンステッド塩基。- B+H+⟶B+Hdisplaystyle ce B + H^+ -> B^+H
- B−+H+⟶BHdisplaystyle ce B^- + H^+ -> BH
- ルイス塩基 (Lewis base)
ルイスの定義による塩基。電子対を与える物質[4]。下式の反応で「B」がルイス塩基。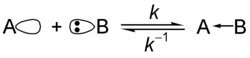
英語 Base の語源
錬金術の用語"the matrix"の類義語として、1717年にフランスの化学者 Louis Lémery が使用したのが最初である[5]。錬金術師のパラケルススは、普遍的な酸か潜在原理が土壌の matrix もしくは wombに含侵することで天然に存在する塩が地中で生まれると主張した。その理論を近代化学に導入したのが フランスの化学者 Guillaume-François Rouelle で、中性塩がアルカリ水溶液等と酸を混ぜ合わせる事で生成されることを明らかにした。18世紀における既知の酸のほとんどが揮発性か蒸留可能な"spirits"で、一方、塩基は酸を「結晶状態の塩か凝固した状態」の形を与え、定着させられる"Base"と考えられた。
出典
^ base - IUPAC Gold Book
^ 『理化学辞典』 第五版, 岩波書店
^ Brønsted base - IUPAC Gold Book
^ Lewis base - IUPAC Gold Book
^ Jensen, William B. (2006). “The origin of the term "base"”. The Journal of Chemical Education 83 (8): 1130. Bibcode 2006JChEd..83.1130J. doi:10.1021/ed083p1130. オリジナルの4 March 2016時点によるアーカイブ。. https://web.archive.org/web/20160304023719/http://www.che.uc.edu/Jensen/W.%20B.%20Jensen/Reprints/129.%20Base.pdf.
関連項目
- 酸と塩基
- 酸
強塩基、超塩基